Bacterial Genetics
Research Lines
Content with Investigacion .
Inmunología Microbiana e Inmunogenética
1. Análisis de la respuesta innata de mamíferos en la infección por Leishmania.
2. Caracterización inmunoproteómica en :
a. Streptococcus suis
b. Lactococcus garviae
c. Mycobacterium spp
3. Desarrollo de inmunoensayos analíticos basados en anticuerpos monoclonales (AcM) para detectar y cuantificar antígenos de origen animal, vegetal y microbiano.
4. Desarrollo y caracterización de AcM frente a los componentes del sistema del Complemento. Aplicación diagnóstica.
5. Desarrollo de reactivos de referencia y diseño de inmunoensayos para la evaluación cualitativa y cuantitativa de toxinas clostridiales.
6. Oferta tecnológica de producción de AcM y policlonales frente a substancias de interés industrial y biomédico.
El grupo está interesado en el estudio de la respuesta inmune desde una perspectiva multidisciplinar que incluye aproximaciones bioquímicas, biotecnológicas, genómicas, inmunoinformáticas y proteómicas, que junto con el uso adicional de modelos in vivo se encaminan al diseño de estrategias terapéuticas frente a diversas enfermedades crónicas, infecciosas y raras que poseen un claro componente inmunológico en su etiología.
Las principales líneas de investigación que está desarrollando el grupo en la actualidad son:
- * Análisis de las respuestas inmunes celulares frente a patógenos virales y bacterianos, mediante técnicas inmunoproteómicas, modelos in vivo con animales transgénicos y muestras humanas.
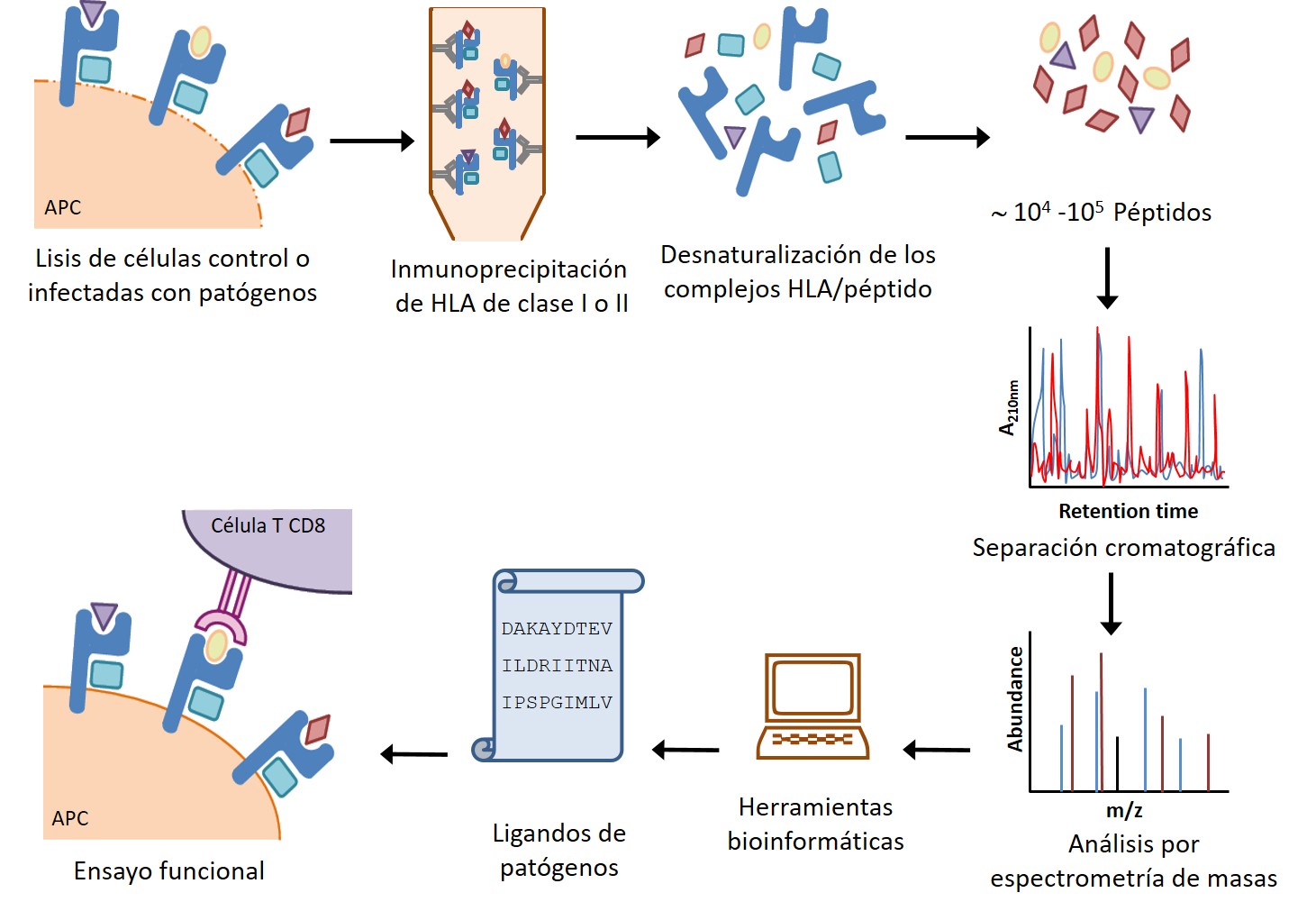
- * Caracterización de CD69: regulación génica, función reguladora inmune en homeostasis e infección y su uso como diana terapéutica, edición génica por CRISPR en modelos animales y celulares, etc.

* Desarrollo de herramientas inmunoinformáticas que permitan analizar la respuesta inmune celular frente a diversos virus de interés sanitario y determinar la eficacia de sus vacunas a nivel de población mundial.

* Estudio de las respuestas inmunes celulares frente a enfermedades raras (artritis reactiva y síndrome del linfocito desnudo) y crónicas (espondiloartropatías).
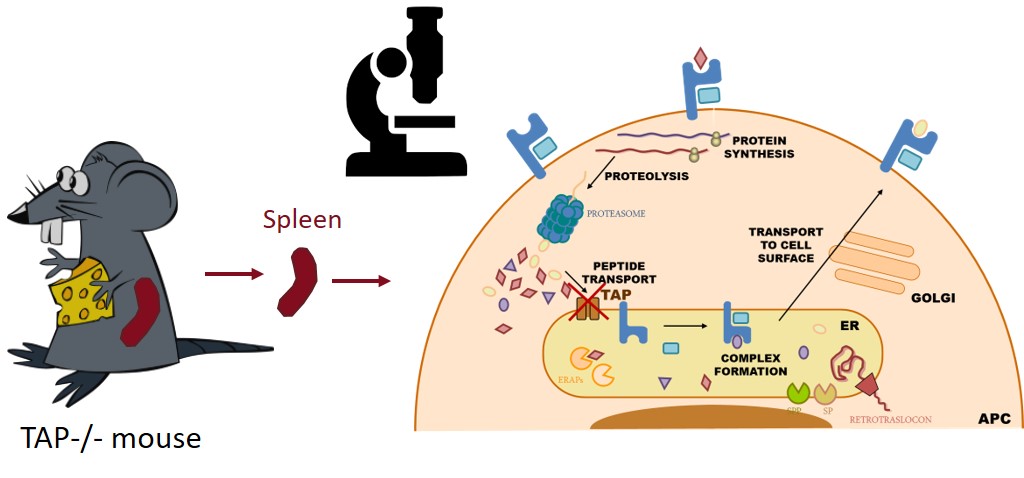
* Inclusión de componentes del sistema inmune en la fabricación de tejidos humanos, especialmente piel, para uso clínico, farmacéutico y cosmético.
- * Generación de virus recombinantes como vectores vacunales.
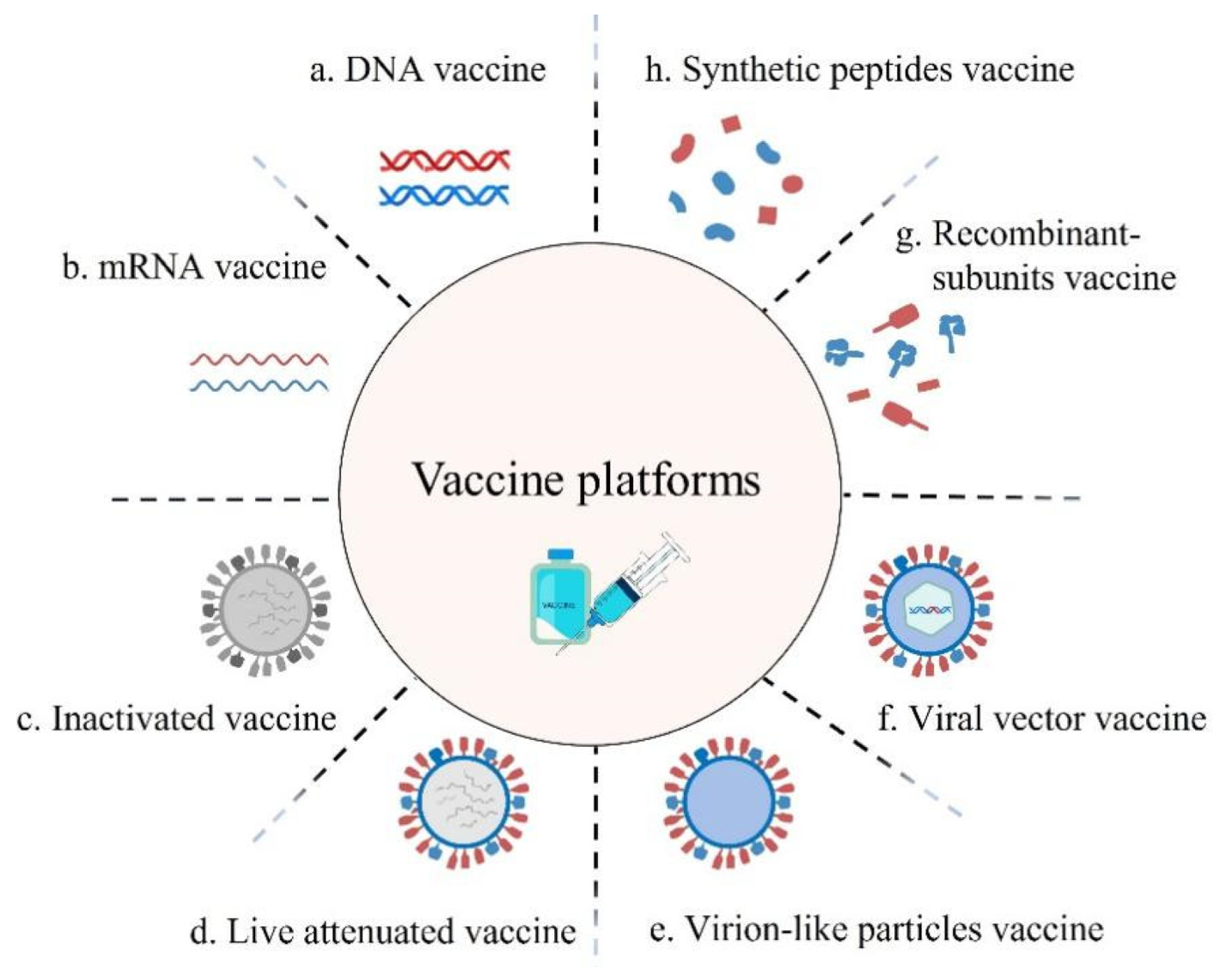
Research projects
Content with Investigacion .
Los proyectos del grupo de los últimos años son los siguientes:
Proyecto “La interrelación de CD69 y el procesamiento antigénico en enfermedades infecciosas y autoinmunes" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2023-2025.
Proyecto “Interacciones génicas y proteicas de CD69 y sus regiones génicas reguladoras con moléculas" financiado por la AEI. Año: 2022-2024.
Proyecto “Nuevas tecnologías de fabricación y optimización de tejidos: la piel como sistema modelo” financiado por el Programa de Actividades de I+D entre grupos de investigación de la Comunidad de Madrid en tecnologías 2018. Año: 2020-2023. Proyecto Coordinado por el Dr. Pablo Acedo de la Universidad Carlos III.
Proyecto “Estudio de CD69 como diana para mejorar el tratamiento de la leucopania y la movilización de células T de memoria de médula ósea" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año:2020-2024.
Proyecto “Diseño racional de una vacuna contra el virus respiratorio sincitial humano” financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2019-2022
Proyecto “Función de CD69 y sus elementos reguladores" financiado por la Acción Estratégica en Salud del Ministerio de Ciencia, Innovación y Universidades. Año: 2017-2022.
Proyecto “Diseño de vacunas recombinantes poliepitópicas para generar respuestas CD8+ contra virus emergentes” financiado por el Plan Nacional de I+D+i del Ministerio de Economía y Competitividad. Año: 2015-2017.
Proyecto “Análisis de los efectos de CD69 dependientes de S1P1 en modelos de infección e inflamación y estudio de su regulación” financiado por el FIS. Año: 2014-2017.
Proyecto “ADELVAC: Adenovirus con delecciones epitópicas para vacunación” financiado por el programa INNPACTO del Ministerio de Economía y Competitividad. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Año: 2012-2014. Proyecto Coordinado por el Dr. Manel Cascallo de VCN BIOSCIENCES SL.
Proyecto “Diseño de vacunas multiepitópicas recombinantes para aumentar la respuesta inmune celular contra el VRSH” financiado por el Plan Nacional de I+D+i del Ministerio de Ciencia e Innovación. Año: 2012-2014.
Publications
Hypervirulent Klebsiella pneumoniae: Epidemiology outside Asian countries, antibiotic resistance association, methods of detection and clinical management
12. Hypervirulent Klebsiella pneumoniae: Epidemiology outside Asian countries, antibiotic resistance association, methods of detection and clinical management. Autores: García-Cobos S, Oteo-Iglesias J, Pérez-Vázquez M. Revista: Enferm Infecc Microbiol Clin (Engl Ed). 2025 Feb;43(2):102-109.
PUBMED DOIRapid cross-border emergence of NDM-5-producing Escherichia coli in the European Union/European Economic Area, 2012 to June 2022
15. Rapid cross-border emergence of NDM-5-producing Escherichia coli in the European Union/European Economic Area, 2012 to June 2022. Autores: Linkevicius M, Bonnin RA, Alm E, Svartström O, Apfalter P, Hartl R, Hasman H, Roer L, Räisänen K, Dortet L, Pfennigwerth N, Hans JB, Tóth Á, Buzgó L, Cormican M, Delappe N, Monaco M, Giufrè M, Hendrickx AP, Samuelsen Ø, Pöntinen AK, Caniça M, Manageiro V, Oteo-Iglesias J, Pérez-Vázquez M, Westmo K, Mäkitalo B, Palm D, Monnet DL, Kohlenberg A. Revista: Euro Surveill. 2023 May;28(19):2300209.
PUBMED DOICharacterization of Carbapenemase-Producing Klebsiella oxytoca in Spain, 2016-2017.
18. Characterization of Carbapenemase-Producing Klebsiella oxytoca in Spain, 2016-2017. Autores: Pérez-Vazquez M, Oteo-Iglesias J, Sola-Campoy PJ, Carrizo-Manzoni H, Bautista V, Lara N, Aracil B, Alhambra A, Martínez-Martínez L, Campos J; Spanish Antibiotic Resistance Surveillance Program Collaborating Group. Revista: Antimicrob Agents Chemother. 2019 May 24;63(6): e02529-18.
PUBMED DOICarbapenemase-Producing Klebsiella pneumoniae From Transplanted Patients in Brazil: Phylogeny, Resistome, Virulome and Mobile Genetic Elements Harboring blaKPC-2 or blaNDM-1.
16. Carbapenemase-Producing Klebsiella pneumoniae From Transplanted Patients in Brazil: Phylogeny, Resistome, Virulome and Mobile Genetic Elements Harboring blaKPC-2 or blaNDM-1. Autores: Raro OHF, da Silva RMC, Filho EMR, Sukiennik TCT, Stadnik C, Dias CAG, Oteo Iglesias J, Pérez-Vázquez M. Revista: Front Microbiol. 2020 Jul 15;11:1563.
PUBMED DOIDissemination of extensively drug-resistant NDM-producing Providencia stuartii in Europe linked to patients transferred from Ukraine, March 2022 to March 2023
17. Dissemination of extensively drug-resistant NDM-producing Providencia stuartii in Europe linked to patients transferred from Ukraine, March 2022 to March 2023. Autores: Witteveen S, Hans JB, Izdebski R, Hasman H, Samuelsen Ø, Dortet L, Pfeifer Y, Delappe N, Oteo-Iglesias J, Żabicka D, Cormican M, Sandfort M, Reichert F, Pöntinen AK, Fischer MA, Verkaik N, Pérez-Vazquez M, Pfennigwerth N, Hammerum AM, Hallstrøm S, Biedrzycka M, Räisänen K, Wielders CC, Urbanowicz P, de Haan A, Westmo K, Landman F, van der Heide HG, Lansu S, Zwittink RD, Notermans DW, Guzek A, Kondratiuk V, Salmanov A, Haller S, Linkevicius M, Gatermann S, Kohlenberg A, Gniadkowski M, Werner G, Hendrickx AP. Revista: Euro Surveill. 2024 Jun;29(23):2300616.
PUBMED DOISpread of the FAR-MRSA clone, a fusidic acid- and meticillin-resistant Staphylococcus aureus ST121, Europe, 2014 to 2024.
19. Spread of the FAR-MRSA clone, a fusidic acid- and meticillin-resistant Staphylococcus aureus ST121, Europe, 2014 to 2024. Autores: Roer L, Yin N, Denis O, Vendrik KE, Zwittink RD, Notermans DW, Perrin M, Khonyongwa K, Tristan A, Youenou B, Layer-Nicolaou F, Werner G, Enger H, Eikrem ECH, Darenberg J, Mäkitalo B, Paulsson M, Björkman J, Fang H, Hallbäck ET, Sundqvist M, Lindholm L, Moganeradj K, García-Cobos S, Cañada-García JE, Holzknecht BJ, Eriksen HB, Hoppe M, Bartels MD, Samaniego Castruita JA, Urth TR, Larsen AR, Petersen A. Revista: Euro Surveill. 2025 Jul;30(28):2500452.
DOICarbapenemase-producing Emergence of NDM-producing Klebsiella pneumoniae and Escherichia coli in Spain: phylogeny, resistome, virulence and plasmids encoding blaNDM-like genes as determined by WGS. aeruginosa in Spain: interregional dissemination of the high risk-clones ST175 and ST244 carrying blaVIM-2, blaVIM-1, blaIMP-8, blaVIM-20 and blaKPC-2
14. Emergence of NDM-producing Klebsiella pneumoniae and Escherichia coli in Spain: phylogeny, resistome, virulence and plasmids encoding blaNDM-like genes as determined by WGS. Autores: Pérez-Vázquez M, Sola Campoy PJ, Ortega A, Bautista V, Monzón S, Ruiz-Carrascoso G, Mingorance J, González-Barberá EM, Gimeno C, Aracil B, Sáez D, Lara N, Fernández S, González-López JJ, Campos J, Kingsley RA, Dougan G, Oteo-Iglesias J; Spanish NDM Study Group. Revista: J Antimicrob Chemother. 2019 Dec 1;74(12):3489-3496.
PUBMED DOIAdditional Information
Streptococcus pneumoniae is a human pathogen that, despite the development of vaccines, continues to be an important cause of mortality and morbidity. We investigate the mechanisms of antibiotic resistance in this bacterium. On the one hand by identifying new therapeutic targets and on the other hand by investigating the molecular basis of the action of antibiotics already used in clinical practice (the fluoroquinolones levofloxacin and moxifloxacin) or not yet used (seconeolitsine). For this purpose, we used a multidisciplinary analysis involving genomics, transcriptomics and proteomics to understand the organization of the S. pneumoniae chromosome and the identification of the factors that stabilize this organization, including ncRNAs. Changes in the level of global supercoiling, either by inhibition of gyrase (decrease) or by inhibition of topoisomerase I (increase) alter the transcriptome. The modulated genes are located in domains, whose genes show specific functional characteristics. The aim is to identify new factors essential for S. pneumoniae physiology and to characterize transcriptional regulation in response to topological stress. In addition, RNA interference technology and CRISPR systems will be used as novel antibacterials. These studies will establish the bases for translational research aimed at the development of new therapeutic targets for the treatment of pneumococcal diseases.
Streptococcus pneumoniae is a human pathogen that, despite the development of vaccines, continues to be an important cause of mortality and morbidity. We investigate the mechanisms of antibiotic resistance in this bacterium. On the one hand by identifying new therapeutic targets and on the other hand by investigating the molecular basis of the action of antibiotics already used in clinical practice (the fluoroquinolones levofloxacin and moxifloxacin) or not yet used (seconeolitsine). For this purpose, we used a multidisciplinary analysis involving genomics, transcriptomics and proteomics to understand the organization of the S. pneumoniae chromosome and the identification of the factors that stabilize this organization, including ncRNAs. Changes in the level of global supercoiling, either by inhibition of gyrase (decrease) or by inhibition of topoisomerase I (increase) alter the transcriptome. The modulated genes are located in domains, whose genes show specific functional characteristics. The aim is to identify new factors essential for S. pneumoniae physiology and to characterize transcriptional regulation in response to topological stress. In addition, RNA interference technology and CRISPR systems will be used as novel antibacterials. These studies will establish the bases for translational research aimed at the development of new therapeutic targets for the treatment of pneumococcal diseases.